
Ernährung und Rosazea
" Da Studien gezeigt haben, dass eine Diät mit vielen (schlechten) Kohlenhydraten die Hautalterung beschleunigt, ist es für mich viel einfacher, den Teller mit Nudeln oder das Weißbrot mit ...

Die im „Gesetz für mehr Sicherheit in der Arzneimittelversorgung“ vorgesehene 3-Jahresfrist ist fast um: Im August könnte eine Regelung Realität werden, wonach biopharmazeutische Medikamente in Apotheken gegeneinander ausgetauscht werden dürfen. Ziel: Kosten im Gesundheitssystem sparen. Doch aktuelle Marktdaten belegen: Der gesetzgeberische Eingriff ist nicht nötig. Und auch der Bundesgesundheitsminister scheint von dem Vorhaben noch nicht überzeugt.
„Bisher entscheiden Arzt oder Ärztin, ob eine Patientin oder ein Patient das Originalprodukt oder das gleichwertige, aber günstigere, Biosimilars bekommt“, erklärt die Arbeitsgemeinschaft ProBiosimilars auf ihrer Website. „Die automatische Substitution ändert das.“ Maßgeblich sind dann am Apothekentisch zwischen Herstellerfirmen und Krankenkassen ausgehandelte Rabattverträge.
Die AG ProBiosimilars hat als Interessenvereinigung der Biosimilar-Hersteller in Deutschland einen Bericht veröffentlicht, der deutlich macht: „Biosimilars gelangen von ganz allein in die Versorgung.“ Soll heißen: Ein Eingriff des Gesetzgebers in den Markt ist unnötig – die Nachfolgepräparate von ehemals patentgeschützten biopharmazeutischen Innovationen setzen sich durch. „Bei den Wirkstoffen, für die es Biosimilars gibt, haben diese einen Versorgungsanteil von durchschnittlich zwei Dritteln.“ Die Folge: „Biosimilars sorgen bereits für massive Einsparungen. Deren Höhe steigt von Jahr zu Jahr steil an. Insgesamt wurden dank Biosimilars schon mehr als vier Milliarden Euro eingespart.“ 2021 waren es allein 1,5 Milliarden Euro. Zusätzlich führen die ausgehandelten Rabattverträge zu weiteren Einsparungen. „Rund 90 Prozent der abgegebenen Packungen von Biosimilars stehen unter Rabattvertrag. Und das ganz ohne automatische Substitution.“

Auch Han Steutel, Präsident des Verbands der forschenden Pharma-Unternehmen (vfa), weiß um den „intensiven Wettbewerb“ und die erzielten „signifikanten Einsparungen“ in diesem Bereich. „Deshalb ergibt es keinen Sinn, dass der Gesetzgeber jetzt den G-BA nötigt, für Biosimilars eine automatische Substitution in den Apotheken zu implementieren.“ Der G-BA (Gemeinsamer Bundesausschuss) ist das höchste Beschlussgremium der gemeinsamen Selbstverwaltung im deutschen Gesundheitswesen.
Laut vfa stehen „den vermeintlichen Sparmöglichkeiten durch so eine Maßnahme […] Bedenken zur Therapiesicherheit gegenüber, etwa weil Ärzt:innen dann nicht mehr wissen, welches Medikament ihre Patient:innen eigentlich erhalten haben.“ Biosimilars sind dem jeweiligen Originalpräparat zwar äußerst ähnlich und in allen klinisch relevanten Parametern wie Wirksamkeit absolut vergleichbar – sie können jedoch nicht identisch sein: Denn sie werden in komplexen Verfahren in lebenden Organismen produziert und unterliegen somit natürlichen Schwankungen.
„[W]enn ein Patient oder eine Patientin hört, dass er aus wirtschaftlichen Gründen ein günstigeres Präparat erhält — ohne dass ihm Arzt oder Ärztin vorher erklärt hat, dass dies problemlos möglich ist — dann wird er skeptisch und möglicherweise dieses Arzneimittel ablehnen. Und dann kann es Nocebo-Effekte geben. Das haben wir in Studien oft genug gesehen“, so Prof. Dr Wolf-Dieter Ludwig, Vorsitzender der Arzneimittelkommission der deutschen Ärzteschaft. Zu Nocebo-Effekten – und entsprechenden negativen gesundheitlichen Folgen – kann es kommen, wenn Patient:innen nicht von der Wirksamkeit eines Arzneimittels überzeugt sind.
Während eines vom forschenden Biotechnologie-Unternehmen Biogen unterstützten „Biotech-Talks“ auf dem Youtube-Kanal „Breaking Lab“ zeigte sich auch Bundesgesundheitsminister Prof. Dr. Karl Lauterbach Ende Juni noch nicht gänzlich überzeugt von einer automatischen Substitution: „Wir werden uns intensiv damit auseinandersetzen“, erklärte er. „In dieser Frage sichten wir derzeit noch die Literatur. Mein Gefühl ist, dass ein größeres Vertrauen hergestellt werden kann, wenn diese Entscheidung zum Schluss bei Ärzten getroffen wird und nicht in der Apotheke.“
Für Dr. Christopher Kirsch, stellvertretender Vorsitzender der AG Pro Biosmilars, ist klar: „Die Politik sollte jetzt innehalten und sich bewusst machen: Noch mehr Einsparungen sind nur auf Kosten der Versorgungssicherheit zu haben.“ Aktuell verteilen sich die Produktionsstätten von Biosimilars über die ganze Welt. Ein weiter verschärfter Kostendruck könnte jedoch dazu führen, dass sie aus Europa abwandern.
Tatsache ist: Sollte Bundesgesundheitsminister Prof. Dr. Karl Lauterbach die automatische Substitution doch noch stoppen wollen, bekäme er ordentlich Rückenwind. Denn abgesehen von den Krankenkassen üben Expert:innen aus den unterschiedlichsten Lagern deutliche Kritik an dem Vorhaben: Auch die deutsche Apothekerschaft hält nichts davon. Und Patient:innen-Vertretungen sind dagegen. In einer durch die Firmen Amgen, Biogen und Pfizer unterstützten Stellungnahme wird etwa Dr. Martin Danner, Bundesgeschäftsführer der BAG-SELBSTHILFE, zitiert: „Aus Sicht der Patient:innen besteht ein intensiver Beratungsbedarf, wenn es um die Anwendung von Biosimilars geht. Es gilt sowohl den Überblick über die verschiedenen Anwendungsverfahren der unterschiedlichen Spritzen und Pens zu behalten, als auch die unterschiedlichen Lagerungsvorgaben zu beachten. In der Folge können Anwendungsfehler und Adhärenz-Probleme auftreten“, so die Warnung. Es braucht daher das „ausführliche Gespräch zwischen Ärzt:innen und Patient:innen“ – diese Situation sei in der Apotheke nicht gegeben.

" Da Studien gezeigt haben, dass eine Diät mit vielen (schlechten) Kohlenhydraten die Hautalterung beschleunigt, ist es für mich viel einfacher, den Teller mit Nudeln oder das Weißbrot mit ...
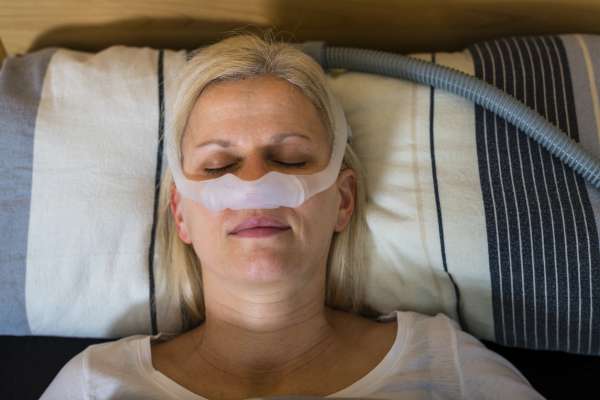
Rosazea-Betroffene, die unter einer Schlafapnoe - Atemstörungen beim Schlaf - leiden, haben Schwierigkeiten nachts mit einer sog. CPAP Sauerstoffmaske zu schlafen, da diese natürlich großflächig sehr ...

OnlineDoctor ist ein bekannter Anbieter für Teledermatologie in Europa. Das Unternehmen wurde 2016 von dem Dermatologen Dr. Paul Scheidegger und den beiden Health-Business-Experten Dr. Tobias Wolf und ...

Ein Leben ohne Gewürze. Eigentlich kaum vorstellbar, oder? Zwar würde uns so das ein oder andere versalzene Gericht erspart bleiben, die Freude am Essen wäre ohne die besondere Note durch das ...

"Wir haben erst wieder einen Termin in drei Monaten." "Wir haben Aufnahmestopp". Klasse Auskunft, wenn ein Schub anliegt. Aber solche analogen Antworten hinter einem brusthohen Empfangs Thresen ...

Die im „Gesetz für mehr Sicherheit in der Arzneimittelversorgung“ vorgesehene 3-Jahresfrist ist fast um: Im August könnte eine Regelung Realität werden, wonach biopharmazeutische Medikamente in ...

Wie Ihr sicher schon gelesen habt, mag ich den Sommer und vor allem die Sonne wirklich gerne. Vielleicht erinnert Ihr Euch an meinen letzten Beitrag, dort habe ich einige Tipps zum Umgang mit ...

Im Rahmen der Interviewreihe „Praxisgespräche" wird fortlaufend das Gespräch zwischen der Deutschen Rosazea Hilfe e.V. (DRH) und Dermatologinnen und Dermatologen aus Klinik und Praxis sowie ...

Ab sofort bietet das Unternehmen Galderma einen innovativen Service für Menschen, die an der Hautkrankheit Rosazea leiden: Auf der neuen Website StellDichDeinerRosacea.de können Rosazea-Patienten ...
Immer aktuelle Infos zu Ihrem Hautthema. Monatlich direkt ins E-Mail-Postfach!